En ny dag med mye interessant stoff, men også mye å fordøye. Det var store temaer som genetikk, vrangforestillinger og antipsykotika.
Hvordan kan genetikk brukes til å forstå schizofreni og andre alvorlige psykiske lidelser?
Først ut i dag var Ole A. Andreassen som er professor ved UiO og psykiater på Ullevål. Han er leder for Norment som er Senter for fremragende forskning.
Han begynte med å gå inn på at det er egentlig liten variasjon i genene hos folk; Vi har 3,2 mrd genkoder og det er under 1% forskjell. Det de som regel leter etter er enten Single Nucleotide Polymorfisme (SNP) hvor f.eks. T er erstattet med G og endringer i antall genkopier (Copy number variation).
Så har vi epigentikken hvor ulike gener er skrudd av eller på; Dette tror man også har betydning for psykiske lidelser, men det er det vanskeligere å finne ut av. F.eks. har man gjort forsøk med mus som har blitt tatt bort fra moren tidlig og sett at man får en endring i genekspresjon av kortisonreseptor. Dette kan gjøre dem mer sårbare for stress. Tilsvarende undersøkelser for genekspresjon er vanskeligere å gjøre hos mennesker da det er behov for å ta hjernebiopsi (og vi kan ikke akkurat ta spedbarn bort fra foreldrene). Man har lurt på om dette er transgenerasjonelt (går i arv), men det virker som at dette “vaskes ut” når man får man får barn (men noe går videre).
Helgenomanalyser blir stadig billigere, kanskje t.o.m. billigere enn å parkere på sykehuset. I USA kan man bestille dette selv, men det er ikke lov i Norge.
Ved hjelp av genom-assosisasjons-studier (GWAS) kan man f.eks. sjekke 10 millioner genvarianter og sammenligne pasienter med friske kontroller. Nå kan man ikke lage flere millioner p-verdier, og de bruker derfor noe som kalles Manhattan plot hvor genomkoordinater plasseres bortover x-aksen, mens man har en logaritmisk skala på y-aksen hvor de laveste p-verdiene (mest signifikant forskjell mellom gruppene) kommer høyest (“skyskraperene i plottet”).
Ved hjelp av dette finner man kanskje 7 varianter som kan gi økt risiko for sykdom, men ved psykiske lidelser er disse gjerne lave for hver enkelt variant (f.eks. 1,2 ganger økt risiko ved én genvariant). For å finne flere samler de flere store studier. Det kommer da helt klart at konseptet med ett gen for schizofreni ikke stemmer. Hver enkelt genvariant har liten effekt, men til sammen blir det mer betydelig.
Flere av genene som ble funnet har med immunsystemet å gjøre. Tidligere har man tenkt at hjernen gjerne var skjermet for immunsystemet (jmf. blod-hjerne-barrieren), mens man nå ser at komplekse interaksjoner mellom immunsystemet, systemisk inflammasjon og hjernen kan føre til endring i humør, kognisjon og atferd (Khandaker et al 2015). Det er flere hypoteser og det trenger ikke å være slk at vi har en infeksjon i hjernen for at den skal bli påvirket.
Flere av genene har med synapsefunksjonen å gjøre (Denver et al – in press), men det er kanskje ikke så overraskende.
Hva betyr det at det er en polygen lidelse? Hver enkeltfaktor er ikke nødvendigvis farlig, men det er summen av det. Kanskje er det ytterpunkter i en normalvariasjon, og hvis man har fått en uheldig sammensetning av genvarianter (som hver for seg kan være vanskelige å skille fra gunstige effekter) så kan man risikere å få en psykisk lidelse.
Mange kjenner til en overlapp mellom kreativitet og bipolar lidelse, men det finner man også ved schizofreni (Power et al 2015, se også boken Touched With Fire). Kan gener som gjør folk mer kreative også føre til at man får en så stor “kreativitet” at det fører til psykose?
I motsetning til hos kvinner hvor eggene er ferdig ved fødselen, så må menn stadig lage nye sædceller. Det ble hevdet at eldre fedre hadde større risiko for å få barn med autisme og schizofreni (Kong et al 2012, se også forskning.no “Barn av modne menn har flere mutasjoner“). I studien fra Island ble det tatt opp at fedrene blir stadig eldre. Dette er riktig hvis man bare ser tilbake til 70-tallet, men går man lengre tilbake i tid var fedrene eldre.
Fra et evolusjonsperspektiv er det en motsetning med at en sykdom er arvelig og samtidig ikke forsvinner. Da må det også være noen grunnleggende positive genvarianter. Gruppen til Andreassen har sett på genomet til sjimpanser og neandertalere sammenlignet med mennesker. Hvor er det flest schizofrenogene genvarianter? Det er mest hos mennesker, så kanskje prisen for å være et menneske med sine egenskaper og evne til tenkning er risikoen for å utvikle psykiske lidelser (Srinivasan et al 2016, omtale på Elsevier, omtale i DailyMail).
Det er genetisk overlapp mellom ulike psykiske lidelser. f.eks. schizofreni og bipolar. Er det kanskje slik at man har en felles sårbarhet og så er det ulike miljøfaktorer som styrer sykdommen?
De har også sett på ulike personlighetstrekk og sammenlignet med sykdom mht felles genvariasjoner. F.eks. er det en sammenheng med schizofreni og åpenhet for nye erfaringer og ADHD og ekstraversjon (men alle funnene her er ikke like signifikante).
Det er også genetisk overlapp mellom mental lidelse og somatisk sykdom. Epidemiologiske og kliniske studier tyder på komorbiditet mellom schizofreni og hjerte-kar-sykdom. I en studie de har gjort (Andreassen et al 2013) fant de ti genloci som er assosiert både med shizofreni og hjerte-kar-sykdom. I hovedsak var dette risikofaktorer som går på triglyserider og HDL og LDL. Dette kan peke i retning at lipid biologi spiller en rolle ved psykiske lidelser. (Man har også hatt mistanke om at antipsykotika også kan virke ved å påvirke lipidmetabolismen/myeliniseringen.)
Disse funnene de har gjort mht genetikk har ingen nytte diagnostisk i dag. De sjeldne genvariantene som gir høy risiko er sjeldne og ikke egnet for screening. De vanlige variantene har liten risiko i seg selv og stor overlapp med friske. Kanskje kan en mer polygenisk risko i fremtiden kunne gi oss en predikasjon på sykdom.
Alt her stemmer med stress-sårbarhetsmodellen. Vi kan ikke gjøre noe med arven, men vi har mulighet til å gjøre noe med miljøet.
Andreassen la også vekt på at vi ikke bør legge genetisk informasjon inn i journalen siden vi ikke vet hva det kan brukes til senere (risiko for psykisk lidelse kan senere vise seg å ha relevans for hjertesykdom eller kreft.
Virkning av antipsykotika – “her og nå”
Nestemann ut var Erik Johnsen, psykiater og professor i Bergen. Han har forsket mye på bruk av antipsykotika og skulle dele litt av kunnskapen sin med oss i dag.
Det er mange antipsykotika på markedet i Norge i dag, men det er viktig å vite at det er større individuelle forskjeller på respons på samme preparat enn det er gruppeforskjeller mellom de ulike preparatene.
Som kjent er hovedeffekten av antipsykotika dopamin-2-reseptor-blokkade (full eller partiell). Den gjeldende teorien for psykose har lenge vært at vi har en hyperdopaminerg situasjon, men det er også mulig at dette bare er endepunktet for en lengre kaskade. Når vi blokkerer dopaminreseptoren gjør vi ikke noe med årsaken til at det var mye dopamin tilstede i utgangspunktet, og kanskje gjør vi det også verre ved at vi får en oppregulering av dopaminreseptorer.
Det er vist at man har forhøyet dopamin allerede i prodromalfasen for psykoselidelser (Howes et al 2009, Howes et al 2011). Oliver Howes som har publisert dette kommer i juni til Bergen Tidlig Psykose Symposium. Howes’ sin gruppe har også funnet at behandlingsresistente (“pasienter som ikke har effekt av antipsykotika”) gjerne har dopaminnivå lik friske kontroller, mens de som responderer på antipsykotika har et høyere nivå. Derimot har de behandlingsresistente høyere glutamatnivå enn både de friske kontrollene og responderene (Demjaha et al 2012). Howes har fremmet en hypotese (Howes & Kapur 2014) hvor man kan klassifisere schizofreni i type A (hyperdopaminerg) og type B (normodopaminerg). Kanskje kan vi senere vite hvem som kan ha effekt av antipsykotika og hvem som kan prøve Leponex (se Goldstein et al 2015 og Stone 2011).
Har antipsykotika selektiv effekt overfor ulike symptomdomener? Det er ulike teorier/modeller, men det ser ut til at det virker på en felles faktor som igjen dekker flere domener (dette forklarer gjerne 80% av effekten). Se Marques et al 2014.
Hvor lang tid tar det før det får effekt? Man har tidligere tenkt at det gjerne tar lang tid før antipsykotika begynner å virke (delayed-onset), men det viser seg at den største endringen skjer som regel i den første uken (early-onset) og mer i de to første ukene enn i de to neste (Agid et al 2003). Dess lenger tid det går uten at vi ser noe særlig effekt, dess mindre sjanse for at det er nyttig.
Antipsykotika virker og numbers needed to treat (NNT) ligger på 2-6 (til sammenligning ligger NNT for antihypertensiva på 125 for å forebygge død, 67 for slag og 100 for å forebygge hjerteinfarkt). Effektstørrelser varier mellom 0,33-0,88 (Leucht et al 2013). Effektstørrelsene for psykofarmaka er omtrent som for medikamenter mot somatiske lidelser (se figur 1 i Leucht et al 2012).
Mht tilbakefallsforebygging så er det 27% som får tilbakefall med medisiner innen 7-12 måneder, mens det er 69% hos dem uten medisiner. Her viste han til studie som anga NNT til 3 og effektstørrelse på 0,9.
Det er en stor “sannhet” innen psykiatrien at alle antipsykotika er like effektive bortsett fra Leponex som skiller seg ut som klart bedre, men sannheten er nok at også amisulprid, olanzapin og risperidon (og kanskje også quetiapin) er noe mer effektiv enn FGA og andre SGA.
Kan resultater fra RCT’er la seg overføre til klinisk praksis? Mange studier er efficacy-studier (egeneffekt), mens flere effektstudier kunne vært nyttig. Det er vanskelig å sammenligne studier også da de gjerne bruker ulike mål på bedring.
Robinson sin studie (Robinson et al 1999) ved førstegangspsykose viste at 87% av pasienten responderte på behandlingen innen 52 uker. Hos en kronisk populasjon er nok dette lavere. En annen studie (Kahn et al 2008) viste en symptomreduksjon på 60% (35 poeng i PANSS). Sinkeviciute m.fl. (ved Bergen psykoseprosjekt, ikke publisert ennå) har sett at 75% av dem som hører stemmer i starten gjør det ikke lenger etter fire uker.
Bivirkninger av antipsykotika
Antipsykotika er veldig effektive medisiner, men det er når vi kommer til bivirkningene at problemene begynner.
Mht vektøkning er det er ikke sånn at alle legger på seg 4 kg, men noen legger ikke på seg i det hele tatt (40%), mens andre legger på seg mer (her viste Johnsen også egne data). 60% merker ingenting til dystoni. For akatasi er det 35% som ikke merker noe, mens 35% merker noe uro uten å ha problemer med å sitte i ro.
Mht forlenget QTc-tid hadde 25% forlenget tid allerede før de fikk medisiner i det hele tatt. På bakgrunn av dette anbefaler de at alle bør ta EKG, noe som er vanlig i bl.a. Danmark. Selv om noen har rykte på seg å være verre enn andre er det ikke spesiell forskjell på olanzapin, risperidon og ziprasidon.
Alvorlige bivirkninger
Malignt nevroleptika-syndrom er sjeldent med insidens på 0,02-0,03% og mortalitet på 5,6%.
Hjerteinfarkt – OR på 1,88 hvis man bruker antipsykotika (Yu et al 2016). Størst de første månedene etter oppstart eller ved korttidsbruk og større ved schizofreni enn andre lidelser.
Plutselig hjertedød – Det er flere mulige virkningsmekanismer her. Antipsykotika kan gi økt QTc-tid kan gi rytmeforstyrrelse, det kan gi karsykdom, påvirkning av det autonome nervesystem med mer. Plutselig hjertedød er en ekslusjonsdiagnose og krever obduksjon. Bruk av antipsykotika gir ca en dobling av risiko, men det er en klar dose-respons sammenheng, og Mellaril (=thioridazin som nå er avregistrert) er verstingen. Dette er alvorlig, men samtidig er det sjeldent, så det gir ikke noen store utslag i total mortalitet.
Økt dødelighet av antipsykotika? – Khan et al 2013 fant en lavere dødelighet blant schizofrene som brukte antipsykotika enn placebogruppen.
Pasienttilfredshet
Johnsen sin gruppe undersøkte hvor tilfredse pasientene var etter at de hadde vært innlagt med psykose (Bø et al 2016). (De ble inkludert etter at utskrivelse var planlagt slik at det ikke skulle bli noe som kunne få konsekvenser for pasientene.) De fant at de fleste av pasientene var tilfredse med behandlingen. Det var lite forskjeller mellom frivillig innlagte og tvangsinnlagte pasienter bortsett fra at den siste gruppen var mer misfornøyd med informasjonen som var blitt gitt. Medvirkningen var det området pasienten var mest misfornøyd med.
Hva betyr antipsykotisk behandling for langtidsforløpet av psykoser?
Forskningsleder Ingrid Melle fra UiO/OUS skulle så bygge videre på Johnsen sitt foredrag. Hun påpekte at hun var ansvarlig for medikamentkapittelet i Nasjonale retningslinjer for behandling av psykoselidelser, så hun tenkte hun kanskje ikke var helt uhildet hvis hun skulle komme til å snakke om retningslinjenes fortreffelighet.
Det har vært et paradigme om at manglende bruk av medikamenter kan skade hjernen (Lieberman 1999). Nå er det nesten over i motsatt paradigme hvor man mener at medisinene kan skade hjernen. Dette er grunnlaget for diskusjonen som har gått i mediene siste par år om bruk av psykofarmaka. Hva skal man tro, og hvem skal man stole på? Hva vet vi om antipsykotisk medikasjon og langtidsforløpet?
Vi vet at det er endringer i hjernen som følge av sykdommen. F.eks. finner man en stor forstørrelse av sideventriklene i forløpet av schizofreni (Kempton et al 2010) og tap av grå substans (Fusar-Poli et al 2013).
De fleste retningslinjer anbefaler bruk av D2-blokkere i akuttfasen. Men det er vanskeligere å si noen mht langtidsforløpet. De fleste er enige om at dette ikke er en kurativ behandling mot en spesifikk sykdom. Vi behandler trolig sekundærfenomener. Det er ikke noen genstudier som peker på at det er noe med dopamin-omsetning eller dopamin-reseptor (et lite unntak) som ligger bak. Så vi driver behandling av symptomer, og når vi snakker om medikamentell behandling av psykose så snakker vi i hovedsak om vrangforestillinger og hallusinose.
Det er vanskelig å si noe om individuelle forløp fordi de er så veldig forskjellige, men fra innkomst til første gangs behandling så har vi en effekt på bedring. Etter det er forløpene mye mer forskjellige. Samler vi opp data fra de første studiene fra 90-tallet som har fulgt opp videre, så ser vi at 80-90% oppnår symptomremisjon etter første psykotiske episode (halvparten ila 3 måneder). Men spørsmålet er hva som skjer videre. I den andre enden av spekteret er det 10-20% som har vedvarende symptomer som aldri får tilbakegang av symptomene sine. 10% får kun én episode, 15% kun to episoder.
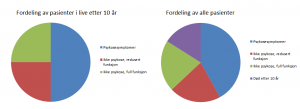
Den norske TIPS-studien (Oslo og Rogaland) viser etter ti år at ca. halvparten har hatt psykosesymptomer siste år, mens den andre halvparten har ikke det. Av den siste halvdelen er det også halvparten av dem igjen (altså en fjerdedel totalt) som har full funksjon. (Dessverre var 16% av deltagerene død etter ti år.)
Vi har ikke RCT av antipsykotika-bruk over 2-3 år. Mens her snakker vi om et tiårsløp av en veldig heterogen gruppe. Gruppen med non-remisjon brukte over tid stadig mer DDD av antipsykotika ila årene (særlig etter to år). De som hører til paradigmet om at medisiner ikke er bra vil gjerne skylde på at de blir dårligere pga mye medisinbruk, men det er slik at symptomene kommer først og så følger medisineringen etter. Samtidig har vi med ulike grupper å gjøre her, at noen blir dårligere uansett hva vi gjør, og noen blir bedre uansett hva vi gjør (hvis vi trekker det litt langt!). Det er ikke noen særlig forskjell i medikamentbruk mellom de tre gruppene.
Funksjonsgjenvinningen skjer som regel tidlig i forløpet (altså for de 25% som klarer seg best), og bildet har lagt seg etter et par år og det vedvarer videre. I studien kunne behandler og pasient etter et års tid velge om de skulle fortsette med protokollen, og kunne gjøre som de vil, så dette representerer i stor grad en vanlig klinisk setting.
Vi har tre scenarier mht utvikling:
- Full behandlingsrespons med få episoder og godt langtidsutfall
- Vedvarende psykotisk symptomatologi på tross av behandling og dårlig langtidsutfall
- Blandet sykdomsbilde med flere epiosder og middels godt langtidsutfall
Vi må vite hvilken pasientgruppe vi snakker om når vi skal diskutere antipsykotika-bruk over tid. Særlig stilles det spørsmål om den første gruppen skal ha videre antipsykotika. Siste gruppen ser vi mye til, men det forskes lite på denne gruppen.
En som har god og rask respons i første episode, vil så bruke lengre tid på å nå symptomfri ved eventuelt tilbakefall (noen av de som responderte godt i episode en, kan respondere dårlig på episode to). Det er derfor man skal være forsiktig med å slutte med antipsykotika for tidlig. Med vedvarende behandling har man mindre risiko for tilbakefall og holder seg i remisjon lengre enn ved bruk av placebo eller intermitterende behandling (de Hert et al 2015).
Så er det motargumentene. Dopaminsensitivisering: Man tenker at det er økt risiko for tilbakefall rett etter seponering, men minkende risiko for tilbakefall over tid. Ved tilbakefall er det da spørsmål om det er oppblomstring av “underliggende” psykose eller er en oppjustering på reseptornivå. Samtidig er det noe merkelig at risikoen er størst for klozapin hvis det er dopaminsensitivsering som ligger til grunn.
Artikkelen til Wunderwink et al fra 2013 er viktig å kjenne til da den stadig kommer frem ifbm diskusjon om medikamentfrie behandlingstilbud selv om den egentlig ikke har med det å gjøre (mer dosereduksjon enn seponering). Halvparten ble randomisert til nedtrapping mens halvparten skulle fortsette etter retningslinjene. Etter 7 år var det bedret funksjon i nedtrappingsgruppen. Vi kan altså oppnå gode resultater på lavere DDD.
Så kommer spørsmålet om effekt på CNS. Man finner en reduksjon i tap av grå substans knyttet til totaleksponering av antipsykotika (Vita et al 2015). Noe av den reduksjonen kan knyttes til sykdommen. I de første studiene ble det tatt med pasienter som brukte FGA, mens vi nå ser flere pasienter over tid som har brukt SGA. Vi finner noe effekt hos de som bruker FGA, men motsatt effekt hos dem som bruker SGA (altså en økning i grå substans). Og da kommer vi inn på diskusjonen rundt myelinisering-hypotesen (“bestemor hadde rett om at det var bra å ha fett på nervene”). Det ser også ut som at disse effektene på CNS ikke er permanente; det er gjort en del rotte- og musestudier på dette.
Når det kommer til mortalitet viser det seg at det faktisk er lavere mortalitet ved bruk av antipsykotika enn ingen antipsykotika. Det var ingen endring for antidepressiver, men økt mortalitet ved bruk av benzodiaepiner. (Tiihonen et al 2015). Her tok Vaaler fra salen opp sin kritikk av Tiihonen fra i går, og mente at studien var imøtegått og man hadde sett på dataene på nytt og kunne ikke konkludere at benzodiazepiner ga økt mortalitet. Til dette svarte Melle at hun ikke nå ville gå i en lang diskusjon med Vaaler, men gi et “tja, ikke akutt” i alle fall.
De som ikke responderer på dopaminblokkere ser ikke ut til å ha den samme oppreguleringen av dopamin (jmf Howes inndeling i hyperdomapinerge og normodopaminerge schizofrenier som Johnsen snakket om i innlegget før (Howes & Kapur 2014)).
Det ble så anbealt en ny artikkel nå om behandlingsresistens i mars-nummeret av American Journal of Psychiatry (Howes et al 2017) som gir retningslinjer for definisjoner av behandlingsresistens, adekvat behandling og behandlingsrespons.
Så hvor går vi fra her? Skal vi skrote den delen av behandlingsretningslinjene som går på vedlikeholdsbehandling? Skader vi pasientene våre ved å anbefale videre bruk av antipsykotika?
Det har vært en stor reduksjon i behovet for psykiatriske sykehussenger siden 1956. Men det finnes også mange forklaringer på hvorfor pasienter i dag klarer seg bedre utenfor sykehus i dag (multifaktorelt). Samtidig, hvis medikamenter skulle skape mer sykdom (som Whitaker hevder), så ville det sett veldig anderledes ut.
Til slutt tok hun opp noen generelle forholdsregler:
- Bruk lavest mulig dose (ikke multifarmasi)
- Gradvise dose-endringer (opp og ned)
- Oppfølging bivirkningsrisiko (særlig hjerte-kar)
De pasienter som kun har hatt én episode med rask tilbakegang av symptomer kan man vurdere avslutning ved stabil remisjon (15% klarer seg bra uten medisiner i naturalistiske studier), og det kan være at det kommer i nye retningslinjer at vi skal avslutte disse raskere enn de to årene som er anbefalt per i dag. Men det legges her vekt på stabil remisjon.
Behandlingsresistens er når man ikke har respons på to adekvate behandlingsforsøk. Er det da lav dopaminaktivitet i utgangspunktet (Howes type B?) eller oppregulering? Da er ikke svaret å øke med dopaminblokkere, men heller forsøke klozapin.
Andre innlegg
Jeg kunne også skrevet om “Utvikling av selvhenførende og persekutoriske vrangforestillinger ved schizofreni i fenomologisk perspektiv” av Peter Handest som var veldig bra, og jeg har notater liggende. Samtidig er det begrenset hva jeg rekker å skrive på kvelden ila psykiatriveka, så jeg skal forsøke å skrive om det senere. Jeg fulgte også etterpå parallelsesjonen som gikk på vrangforestillinger og jeg håper jeg også får skrevet om det senere. Jeg har derfor valgt å kalle dette innlegget for dag 4 – del 1.

Veldig imponerende hvor mye du får med deg av forelesningene og evner formidle videre på en så pedagigisk måte, attpåtil skrevet samme kveld. Hatten av!
Takk for det!
Et av problemene er at studier av korttidseffekt og vedlikeholdsmedisinering er ikke rene placebogrupper uten medisin, men placebogruppen er blant pasienter som har tatt psykofarmaka f. eks. et år og blir så tatt av medisinen, dvs. her vises også avvenningssymptomer. Er det sykdommen som kommer tilbake eller er det avvenningssymptomer? Her er det muligheter for reduksjon av doser: Kunnskaps- og forskningsbasert avvikling av nåværende helseskadelige overmedisering i psykiatrien til fordel for evidensbasert helsefremmende praksis http://home.broadpark.no/~wkeim/files/Aapent_brev_kunnskap-uv.html